Le tableau périodique des éléments
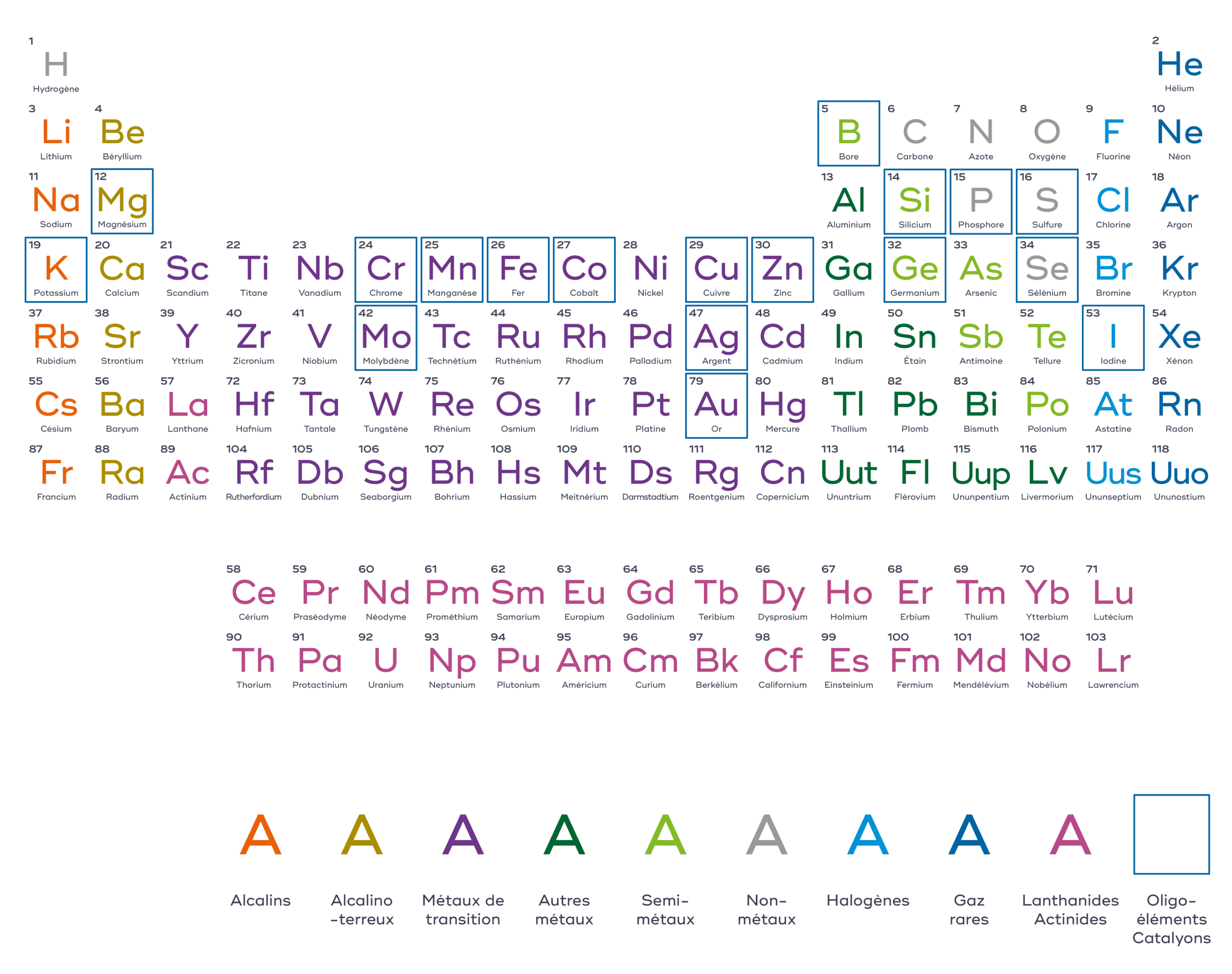
Vous l’avez sans doute déjà vu quelque part : le tableau périodique des éléments. Parce qu’il est aussi mystérieux qu’il est utile, nous vous proposons d’en percer tous les secrets. Découvrez cet incontournable outil scientifique ainsi que le rôle des oligo-éléments sur votre santé.

Le tableau périodique des éléments répertorie tous les éléments chimiques connus qui constituent le monde qui nous entoure. Ils sont classés par numéro atomique croissant (c’est-à-dire le nombre de protons contenus dans l’atome, qui est propre à chaque élément), et organisés en fonction de leur configuration électronique et de leurs propriétés chimiques.
Cette classification particulière a été conçue par Dmitri Ivanovich Mendeleïev à la fin du XIXème siècle.
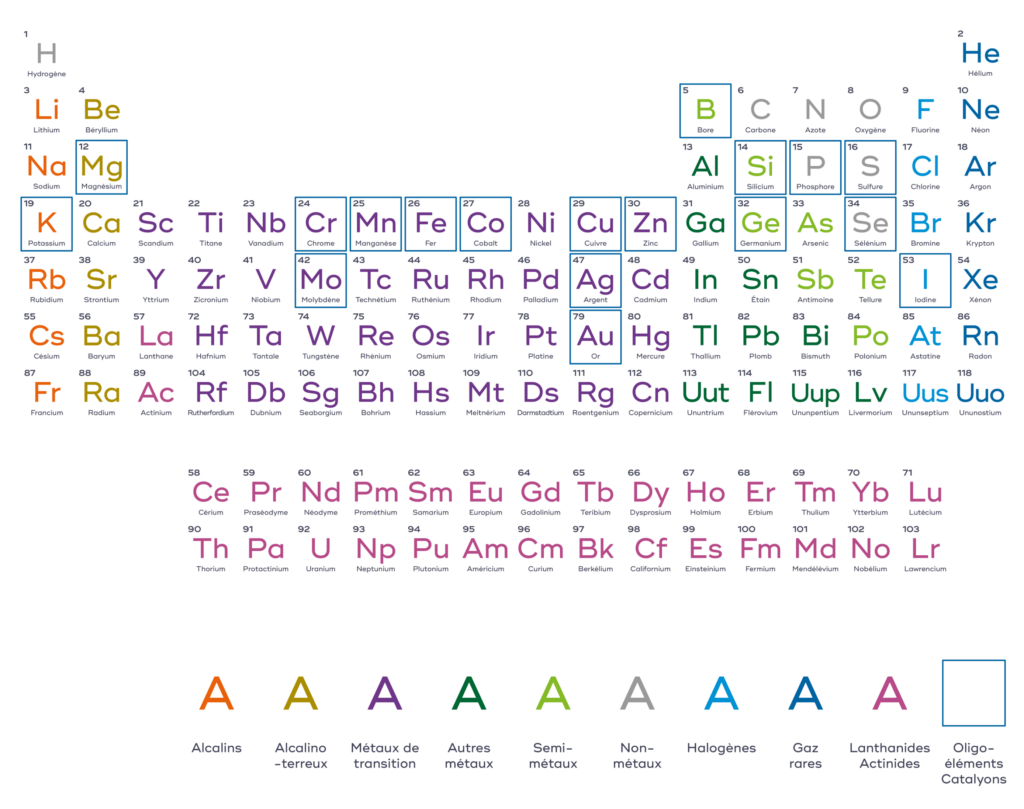
Les oligo-éléments du tableau periodique peuvent etre regroupés par familles, représentées en couleur sur le tableau ci-dessous, partageant certaines propriétés physiques et chimiques. Retrouvez également les oligo-éléments Catalyons et leur specificités ci-dessous.
On retrouve les oligo-éléments Catalyons dans plusieurs familles d’éléments du tableau périodique. Retrouvez le rôle des familles d’oligo-éléments ci-dessous.
Les Alcalins
Cette famille regroupe des métaux. Ce sont des solides mous, coupables au couteau et sont de très bons conducteurs d’électricité et de la chaleur. Ils sont peu utilisés à l’état pur à cause de leur extrême réactivité chimique. Liés à d’autres éléments, ils peuvent être retrouvés par exemple dans les batteries (Lithium) ou encore dans le sel de table (Sodium). Le potassium (K) est un oligoélément qui fait partie de la famille des Alcalins.
Les Alcalino-terreux
Cette famille regroupe des métaux, que l’on retrouve dans la composition de nombreuses roches, d’où leur nom. Ils sont moins mous et moins réactifs que les alcalins. Ils sont bons conducteurs d’électricité et de chaleur. Ils sont beaucoup utilisés dans les pièces pyrotechniques (feux d’artifices) et jouent un rôle important chez les êtres vivants.
Les métaux de transition
Cette famille regroupe des métaux pour la plupart. Les métaux de transition contiennent les éléments les plus malléables et ductiles, comme l’or, l’argent et le platine. Les métaux de transition ont tendance à fondre et à bouillir à des températures plus élevées que les autres familles, sont d’excellents catalyseurs, et montrent une grande variété de couleurs à l’état solide et au contact de l’eau.
Les autres métaux
Hormis l’aluminium, cette famille regroupe des métaux plutôt mous, avec une température de fusion et d’ébullition inférieure à celles des métaux de transition. Ils sont pour la plupart utilisés dans l’industrie mais avec la découverte de leur toxicité sur le système nerveux de l’humain et sur l’environnement, leur usage est de plus en plus réglementé et limité.
Les semi-métaux
Les semi-métaux, appelés aussi métalloïdes, sont des éléments qui possèdent des propriétés métalliques et/ou non-métalliques. Ils sont fragiles et médiocres conducteurs d’électricité. Ils sont largement utilisés dans les composantes électroniques comme semi-conducteurs, et sont généralement utilisés à travers leurs alliages avec des métaux.
Les non-métaux
Bien qu’ils soient moins présents dans le tableau que les métaux, les non-métaux sont les constituants majeurs de tous les êtres vivants : l’hydrogène, le carbone, l’azote, l’oxygène et le phosphore sont des éléments principaux des molécules biologiques.
Les Halogènes
Cette famille regroupe des éléments non-métaux, très colorés, bactéricides et extrêmement réactifs. On les retrouve donc toujours liés à d’autres éléments chimiques dans la nature. C’est la famille qui est la seule à posséder des éléments dans chacun des trois états à température ambiante (gazeux, liquide et solide).
Les gaz rares
Cette famille regroupe uniquement des éléments qui sont sous forme de gaz à l’état pur. Ils sont très peu réactifs et sont relativement rares dans l’atmosphère terrestre. Ils sont incolores à l’état naturel mais produisent de la lumière colorée lorsqu’ils sont soumis à une tension électrique.
Les Lanthanides Actinides
Cette famille regroupe des métaux mous aux reflets argentés qui ternissent rapidement à l’air libre. Certains sont facilement coupables au couteau. Ils sont réactifs, radioactifs et toxiques pour le corps humain.